Το γλοιοβλάστωμα (glioblastoma IDH1 wild type) αποτελεί την πιο κακοήθη μορφή των γλοιωμάτων, που είναι πρωτοπαθείς όγκοι του εγκεφάλου. Εντάσσεται στους όγκους βαθμού κακοήθειας 4 σύμφωνα με τον ΠΟΥ (Παγκόσμιος Οργανισμός Υγείας), και υποδηλώνει ότι ο όγκος ξεκίνησε de novo, δηλαδή δεν προϋπήρχε στην περιοχή κάποιος όγκος χαμηλότερης κακοήθειας που εξελίχθηκε. Το αστροκύττωμα βαθμού κακοήθειας 4 κατά ΠΟΥ, (astrocytoma IDH1 mutated) έχει μια ελαφρά καλύτερη πρόγνωση από το γλοιοβλάστωμα και προέρχεται από αστροκυττώματα χαμηλότερης κακοήθειας που προϋπήρχαν. Ουσιαστικά έχει επικρατήσει να χρησιμοποιείται λανθασμένα ο όρος γλοιοβλάστωμα και για τις δύο παραπάνω ασθένειες, για τον λόγο ότι ο διαχωρισμός τους έγινε πρώτη φορά στην τελευταία αναθεώρηση της ταξινόμησης των εγκεφαλικών όγκων το 2021.
Η ετήσια επίπτωση των γλοιοβλαστωμάτων ή αστροκυττωμάτων βαθμού κακοήθειας 4, δηλ. ο αριθμός των νέων περιστατικών με τις ασθένειες αυτές ανά 100.000 πληθυσμό ανά έτος ανέρχεται σε περίπου 4 νέους ασθενείς/100.000 κατοίκους/έτος τόσο σε αμερικανικά όσο και ελληνικά καταγραφικά συστήματα (Ostrom QT, 2023; Gousias K, 2009). Οι παραπάνω όγκοι είναι οι πιο συχνοί από τα γλοιώματα, καθώς αποτελούν το 51 % όλων των γλοιωμάτων. Για τον λόγο ότι οι όγκοι αυτοί είναι εξαιρετικά επιθετικοί, η θεραπεία τους επιβάλλεται να είναι άμεση.
Ο Καθηγητής Νευροχειρουργικής Δρ. Γούσιας έχει υπερεξειδίκευση στη χειρουργική αντιμετώπιση γλοιοβλαστωμάτων και γλοιωμάτων, αφού έχει πραγματοποιήσει περισσότερες από 800 επεμβάσεις σε ασθενείς με γλοιώματα στην Γερμανία. Αυτήν την τεχνογνωσία, που παρείχε επί σειρά ετών σε κορυφαία κέντρα Νευροχειρουργικής της Γερμανίας, όπου θήτευσε τα τελευταία 5 χρόνια ως διευθυντής μεγάλης Aκαδημαϊκής Νευροχειρουργικής Κλινικής του Πανεπιστημίου του Münster, πλέον την προφέρει και στην Ελλάδα, μέσω του Ιατρικού Κέντρου Αθηνών.
Στα πλαίσια της αναγνώρισης του κλινικού και ακαδημαϊκού του έργου πάνω στα γλοιώματα έχει επιλεγεί από το 2023 ως ειδήμων χειρουργός όγκων εγκεφάλων στην 15μελή επιτροπή της Ευρωπαϊκής Νευροχειρουργικής Εταιρείας (EANS Neurooncology section).
Τα ακριβή αίτια της ανάπτυξης των γλοιοβλαστωμάτων και γλοιωμάτων γενικότερα δεν είναι πλήρως κατανοητά. Υπάρχουν λίγοι γνωστοί καθορισμένοι παράγοντες κινδύνου. Η ακτινοβολία, ιδιαίτερα η ιονίζουσα ακτινοβολία, έχει αναγνωριστεί ως πιθανός παράγοντας κινδύνου για την ανάπτυξη όγκων του εγκεφάλου όπως το γλοιοβλάστωμα. Άτομα που έχουν εκτεθεί σε ορισμένες πηγές ακτινοβολίας, όπως ιονίζουσα ακτινοβολία, επαγγελματικά ή ιατρικά (π.χ. ακτινοθεραπεία για θεραπεία καρκίνου), μπορεί να διατρέχουν αυξημένο κίνδυνο να αναπτύξουν αυτόν τον τύπο όγκου. Έπειτα, υπάρχει η τάση για ανάπτυξη των όγκων αυτών στα πλαίσια διαφόρων συνδρόμων , όπως για παράδειγμα στην περίπτωση της νευροϊνωμάτωσης, μια γενετική διαταραχή που επηρεάζει το νευρικό σύστημα. Ωστόσο, αυτοί οι παράγοντες κινδύνου δεν ισχύουν για τους περισσότερους ασθενείς.
Η τρέχουσα εστίαση είναι στην οικογενειακή προδιάθεση, δηλαδή στην τάση μιας οικογένειας ή ορισμένων μελών της οικογένειας να αναπτύξουν μια συγκεκριμένη ασθένεια ή διαταραχή (Melin BS, Gousias K, 2017; Kinnersley B, Gousias K, 2015A; Kinnersley B, Gousias K, 2015B; Jacobs DI, Gousias K, 2012). Αυτή η τάση επηρεάζεται από γενετικούς παράγοντες και μπορεί να έχει ως αποτέλεσμα τα μέλη της οικογένειας να έχουν αυξημένο κίνδυνο να αναπτύξουν μια συγκεκριμένη ασθένεια με βάση γενετικές προδιαθέσεις. Περισσότερα από 50 γονίδια έχουν ήδη αναγνωριστεί για το σκοπό αυτό (Enciso-Mora V, Gousias K, 2013A; Enciso-Mora V, Gousias K, 2013B; Kinnersley B, Gousias K, 2016; Sanson M, Gousias K, 2011). Αυτή η αιτιολογία είναι ωστόσο υπεύθυνη μόνο για περίπου το 4% των περιπτώσεων. (Simon M, Gousias K, 2011). Επομένως, η αιτία του όγκου παραμένει ασαφής για τη συντριπτική πλειοψηφία των ασθενών.
Όπως ισχύει και με τους λοιπούς όγκους, κυρίως η εντόπιση και το μέγεθος του όγκου καθορίζει και τα συμπτώματα που προκαλεί στον ασθενή. Τυπικά συμπτώματα είναι για παράδειγμα, επιληπτικές κρίσεις, νευρολογικά ελλείμματα όπως παράλυση στην μια πλευρά του σώματος, διαταραχές στην ομιλία ή στην κατανόηση, οπτικές διαταραχές ή απλά διαταραχές προσωπικότητας και βυθιότητα. Συχνά εμφανίζονται επίσης μη ειδικά συμπτώματα, όπως πονοκέφαλοι ή ζάλη.
Η σίγουρη και τελική διάγνωση των όγκων αυτών γίνεται μέσω της βιοψίας και της επακόλουθης ιστολογικής και μοριακής εξέτασης, καθώς στην συντριπτική πλειοψηφία τους, ενδείκνυται η χειρουργική αφαίρεσή τους, όταν αυτό είναι δυνατό να γίνει με ασφάλεια. Προηγουμένως ενδείκνυται να διενεργηθούν διάφορες απεικονιστικές μέθοδοι. Αναγκαία είναι τουλάχιστον μια μαγνητική τομογραφία εγκεφάλου με σκιαγραφικό, η οποία θα θέσει την σοβαρή υποψία για όγκο εγκεφάλου και δύναται με μεγάλη πιθανότητα να προβλέψει έναν κακοήθη εγκεφαλικό όγκο.
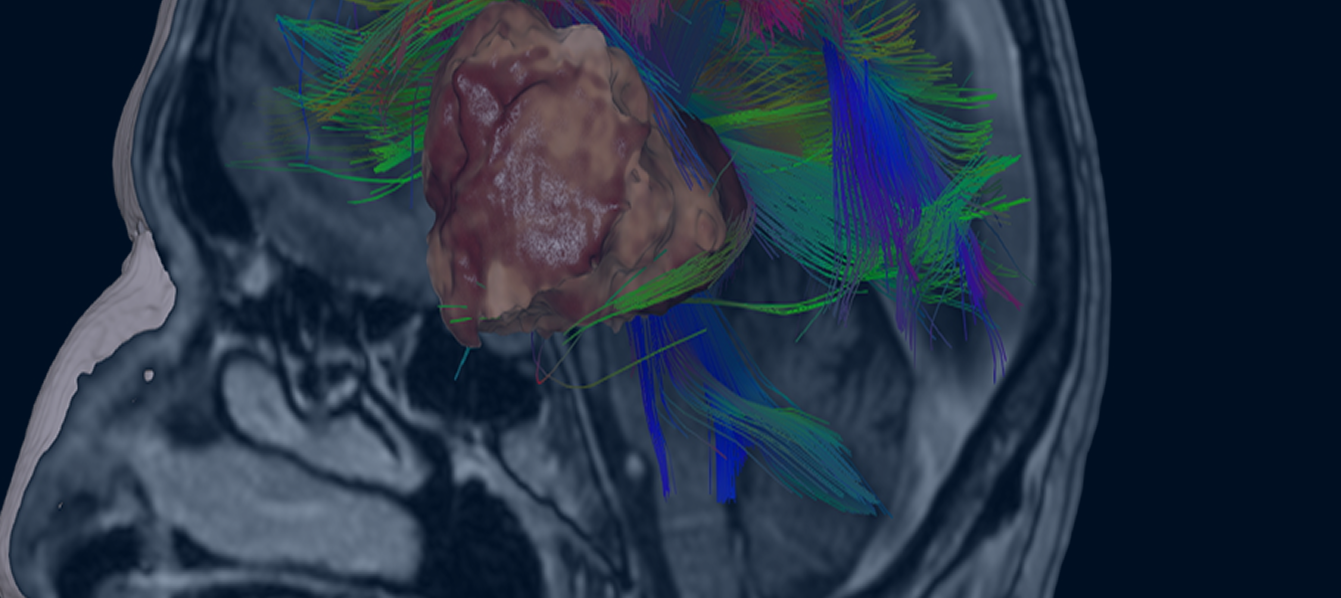
Ειδικές μαγνητικές, όπως φασματοσκοπία βοηθούν στην μελέτη του μεταβολισμού των όγκων, δίνοντας κάποια επιπλέον πληροφορία για να διαγνώσουμε έναν όγκο χαμηλής ή υψηλής κακοήθειας. Η μαγνητική δεσμιδογραφία είναι αναγκαία σε πολλές περιπτώσεις για την σωστή προετοιμασία για το χειρουργείο.
Η πρόγνωση των ασθενών με γλοιοβλαστώματα εξαρτάται από πολλούς παράγοντες, τόσο από τα βιολογικά χαρακτηριστικά του ίδιου του όγκου (Gousias K, 2010; Gousias K, 2012; Gousias K, 2013; Gousias K, 2014A; Gousias K, 2014B; Martinez R, Gousias K, 2018; Gousias K,2022) αλλά κυρίως από τον βαθμό αφαίρεσης του όγκου κατά τη διάρκεια του χειρουργείου (Gousias K, 2014C; Gousias K, 2018). Με δεδομένο ότι δεν μπορούμε να επηρεάσουμε τα βιολογικά χαρακτηριστικά του όγκου, εστιάζουμε κυρίως στον βαθμό εξαίρεσης του όγκου.
Παρακάτω θα παρουσιασθούν ορισμένα περιστατικά με γλοιοβλάστωμα σε κρίσιμες περιοχές για τις λειτουργίες του εγκεφάλου για την αντιμετώπιση των οποίων είναι πολύ πιθανό να προταθεί από συνάδελφους νευροχειρουργούς, νευρολόγους ή ογκολόγους μια πιο συντηρητική και αμυντική χειρουργική τεχνική, όπως μόνο μια βιοψία ή μια μερική αφαίρεση του όγκου. Η δική μας στρατηγική είναι σαφέστατα διαφορετική. Τυπικά παραδείγματα γλοιοβλαστωμάτων στα οποία μια ολική εξαίρεση ήταν δυνατή και ταυτόχρονα ασφαλής ενώ αυτό αρχικά δεν φάνταζε πολύ πιθανό δίνονται στην συνέχεια.
Το δόγμα της σύγχρονης χειρουργικής όγκων απεικονίζεται στις μαγνητικές αυτές. Στόχος μας είναι η μέγιστη δυνατή ασφαλής αφαίρεση του όγκου. Δεν πρέπει να στοχεύουμε στην εξαίρεση όχι μόνο του όγκου, όπως φαίνεται στην μαγνητική αλλά και στην αφαίρεση και της διηθητικής ζώνης και της υγιούς περιβάλλουσας περιοχής αν αυτή δεν έχει λειτουργίες. Η εικόνα 1α είναι προεγχειρητική, εδώ έχει σχεδιασθεί το εύρος της στοχευμένης εξαίρεσης. Η εικόνα 1β δείχνει το μετεγχειρητικό αποτέλεσμα μιας υπερολικής εξαίρεσης. Πρόκειται για την πρώτη ασθενή που χειρουργήθηκε στην Ελλάδα από τον Καθ. Γούσια τον Οκτώβριο του 2023, η οποία διαγνώσθηκε με την πιο επιθετική μορφή του γλοιοβλαστώματος, το λεγόμενο γλοιοσάρκωμα, η οποία 20 μήνες μετά την χειρουργική επέμβαση παραμένει χωρίς ένδειξη όγκου στην μαγνητική και το πιο σημαντικό χωρίς νευρολογικά ελλείμματα.
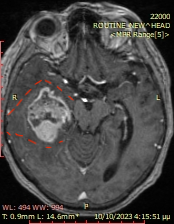
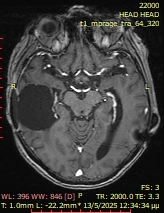
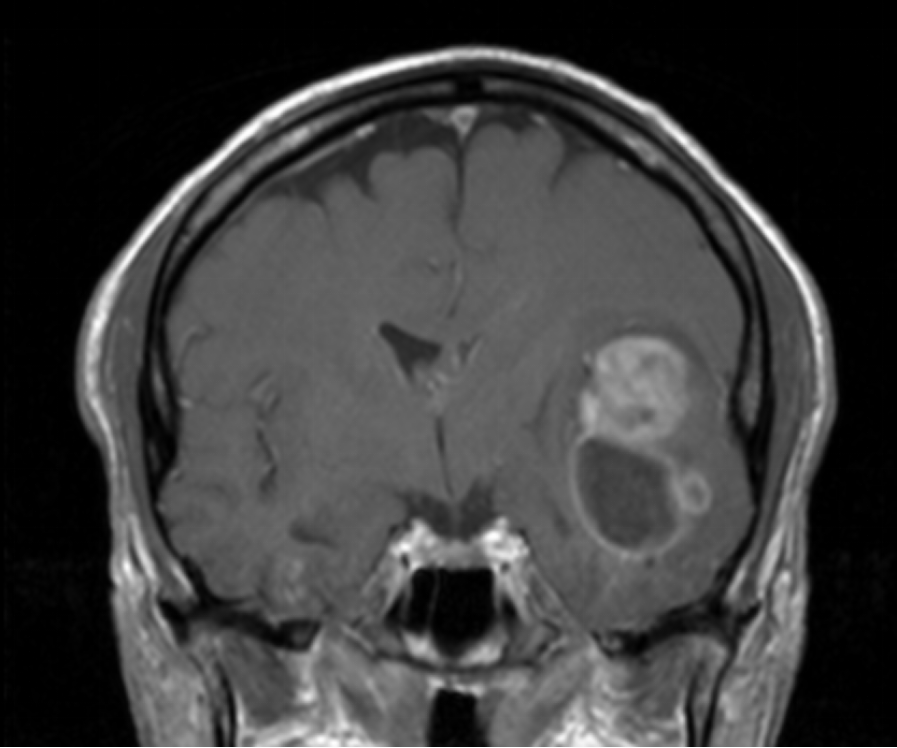
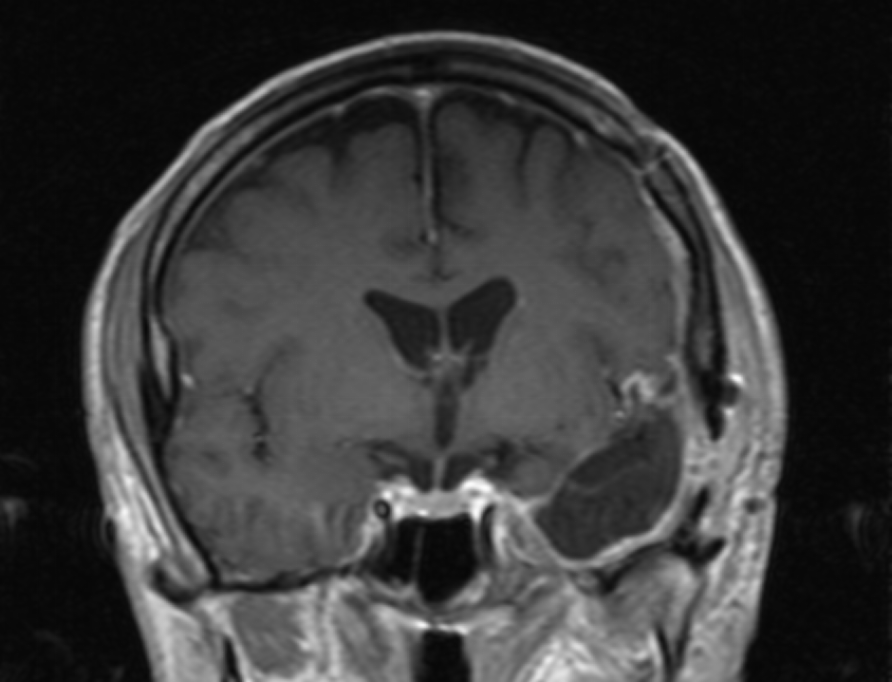
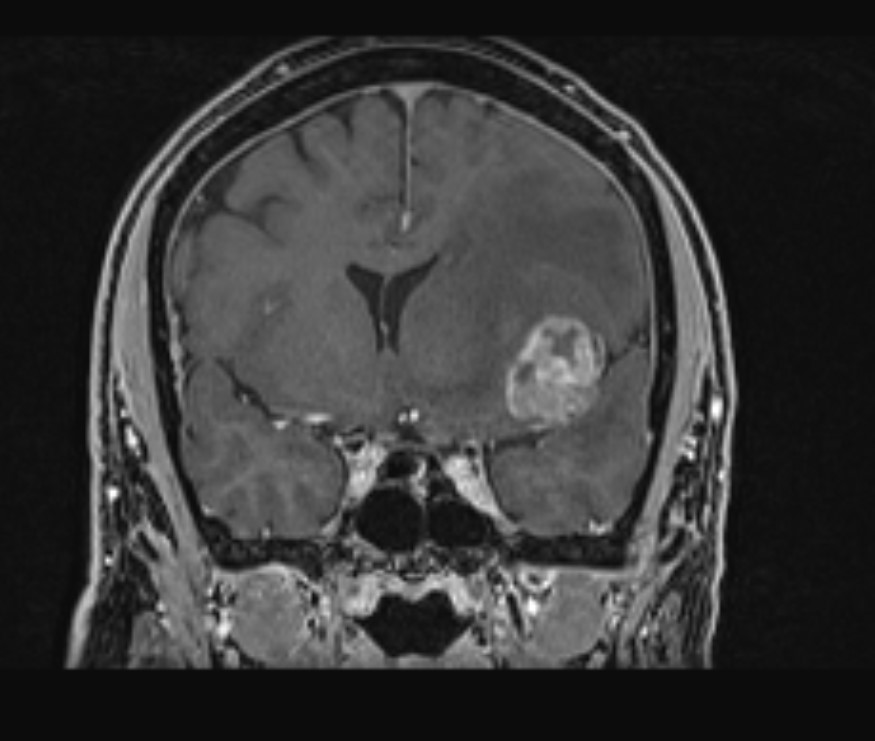
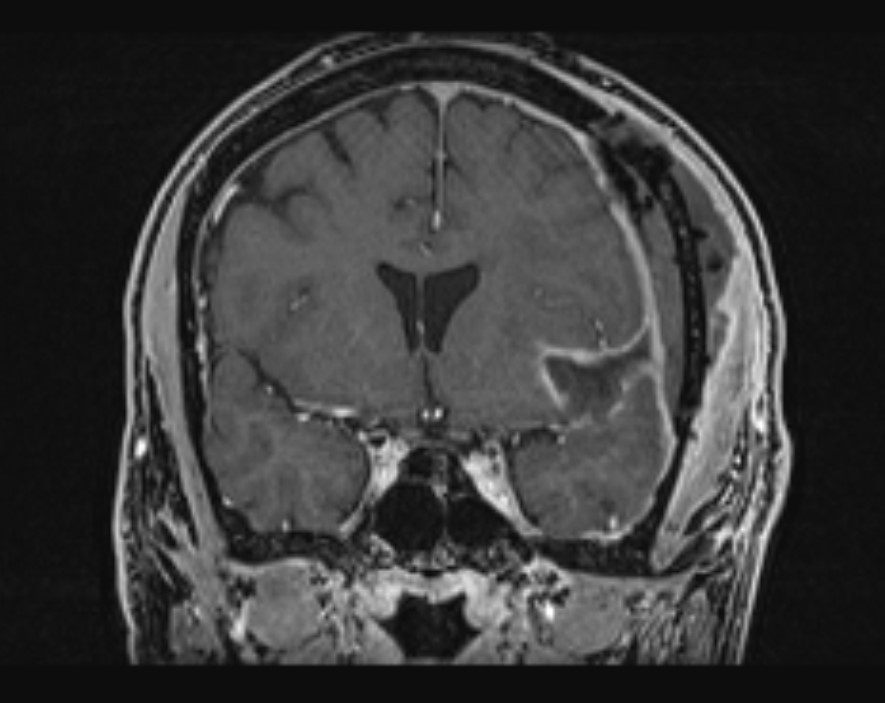
Η αφαίρεση του όγκου μέσω χειρουργικής επέμβασης είναι σχεδόν πάντα το πρώτο βήμα για τη θεραπεία του γλοιοβλαστώματος ή του αστροκυττώματος βαθμού κακοήθειας 4. Ο στόχος είναι να αφαιρεθούν όσο το δυνατόν περισσότερα κύτταρα όγκου χωρίς να επηρεαστεί ο υγιής εγκεφαλικός ιστός. Ωστόσο, σε ορισμένες περιπτώσεις η πλήρης αφαίρεση είναι δυνητικά επικίνδυνη όταν τα γλοιοβλαστώματα αναπτύσσονται διηθητικά στον περιβάλλοντα ιστό, ο οποίος έχει σημαντικές λειτουργίες, όπως την ομιλία, την κατανόηση, την κίνηση κτλ. Σε αυτές τις περιπτώσεις πρέπει να εξαντλήσουμε ΔΙΕΓΧΕΙΡΗΤΙΚΑ κάθε πιθανότητα για αφαίρεση περισσότερου καρκινικού ιστού χωρίς να βλάψουμε τον ασθενή.
Από τη στιγμή που υπάρχει υποψία για γλοιοβλάστωμα, θέλουμε να πραγματοποιήσουμε την επέμβαση το συντομότερο δυνατό, συνήθως 2-3 ημέρες αργότερα αφού έχει εκφραστεί μια υποψία. Χρειαζόμαστε καλή προετοιμασία για αυτό, πράγμα που σημαίνει πολλά δεδομένα απεικονιστικά, όχι μόνο από τον ίδιο τον όγκο, αλλά και από άλλες περιοχές, δεσμίδες και νευρικές οδούς στον εγκέφαλο, ώστε να μπορούμε να προσδιορίσουμε την ακριβή θέση του όγκου και τη συνάφειά του με τις εγκεφαλικές λειτουργίες. Αυτό είναι σημαντικό και για τη χειρουργική τεχνική και προσπέλαση, για την όλη διαδικασία. Για παράδειγμα, υπάρχουν επιφανειακά εντοπισμένοι όγκοι που μπορούν απλά να αφαιρεθούν πλήρως και ριζικά. Και μετά υπάρχουν εκείνα που είναι κοντά στις κινητικές δεξιότητες και τη γλώσσα. Δεν μπορούμε απλώς να τα αφαιρέσουμε χωρίς μέτρα προφύλαξης. Σε τέτοιες περιπτώσεις επιλέγουμε επιπλέον τεχνικές παρακολούθησης της εγκεφαλικής λειτουργίας και της λειτουργικής νευροανατομίας, όπως η καθευτή νευροπαρακολούθηση, η διεγχειρητική νευροπλοήγηση με απεικόνιση των δεσμίδων ή ένα χειρουργείο με ασθενή σε εγρήγορση. Κατά τη διάρκεια μιας επέμβασης με ασθενή σε εγρήγορση, μπορούν να εντοπιστούν κρίσιμες περιοχές του εγκεφάλου, οι οποίες θα προφυλαχθούν, ώστε να πραγματοποιηθεί η καλύτερη εκτομή των λοιπών δομών.
Ο βαθμός εξαίρεσης του όγκου είναι αποφασιστικός για την μετέπειτα πορεία του ασθενούς. Ασθενείς με υψηλής αλλά και αυτοί με χαμηλής κακοήθειας γλοιώματα στους οποίους ο όγκος έχει αφαιρεθεί πλήρως εμφανίζουν καλύτερη πρόγνωση σε σχέση με τους ασθενείς στους οποίους έχει αφαιρεθεί μερικώς ή έχουν οδηγηθεί σε μια απλή βιοψία (Stummer W, 2008; Gousias K, 2014C; Gousias K, 2018). Σήμερα υπάρχουν διάφορες διεγχειρητικές τεχνικές, που μας υποστηρίζουν στο στόχο μας, να αφαιρέσουμε όσο περισσότερο καρκινικό ιστό, αν γίνεται ιστό ακόμα και από την περιοχή γύρω από τον όγκο, που ονομάζουμε διηθητική ζώνη.
Μερικές σύγχρονες διεγχειρητικές τεχνικές, είναι:
Ο συνδυασμός λοιπόν ενός ασφαλούς χειρουργείου με ταυτόχρονη ολική αφαίρεση του όγκου αποτελεί τον στόχο της σύγχρονης χειρουργικής νευρο-ογκολογίας. Αυτό είναι σαφέστατα πιο πιθανό να προσφερθεί από ειδήμονες νευροχειρουργούς (Gousias K, 2024) με ειδική εκπαίδευση σε μεγάλα κέντρα, μεγάλη χειρουργική εμπειρία και εξειδίκευση στην χειρουργική των όγκων καθώς και διεθνή αναγνώριση τους. Η επιτροπή Χειρουργικής Νευρο-ογκολογίας της Ευρωπαϊκής Νευροχειρουργικής Εταιρείας δημοσίευσε το προφίλ ενός expert χειρουργού για όγκους εγκεφάλου και νωτιαίου μυελού (Gousias K, 2024).
Η επιλογή της βέλτιστης επικουρικής θεραπείας εξαρτάται από την ατομική κατάσταση του ασθενούς, την μοριακή βιολογία του όγκου και τις συστάσεις της θεραπευτικής ομάδας μετά από συνεδρία του νευρο-ογκολογικού συμβουλίου. Ο συνδυασμός χειρουργικής επέμβασης, ακτινοθεραπείας και χημειοθεραπείας είναι η τυπική θεραπεία για το γλοιοβλάστωμα, αλλά μπορεί επίσης να ληφθούν υπόψη και άλλες θεραπευτικές επιλογές. Είναι σημαντικό να συνεργαστεί η ιατρική ομάδα για την ανάπτυξη εξατομικευμένης θεραπείας και να ληφθούν υπόψη οι πιο πρόσφατες έρευνες και κλινικές μελέτες.
Σε περίπτωση γλοιοβλαστώματος με μεθυλιωμένο τον υποκινητή του γονιδίου MGMT, η καθιερωμένη επικουρική θεραπεία ορίζεται από το πρωτόκολλο Stupp, το οποίο προβλέπει την αρχική συνδυαστική χημειο- (τεμοζολομίδη) και ακτινοθεραπεία (60 Gy) για 6 συνεχόμενες εβδομάδες (ΔΕ-ΠΑ), η οποία αναμένεται να ξεκινήσει 4 εβδομάδες μετά την χειρουργική επέμβαση. Μετά το πέρας της συνδυαστικής χημειο/ακτινοθεραπείας, προβλέπονται 6 κύκλοι χημειοθεραπείας με τεμοζολομίδη. Ο κάθε κύκλος αποτελείται από 28 ημέρες, στις πρώτες 5 ημέρες λαμβάνεται το φάρμακο στην οικία του ασθενή, στις επόμενες 23 γίνεται παύση του φαρμάκου. Πριν την αρχή του νέου κύκλου γίνονται αιματολογικές εξετάσεις, για να επιτραπεί η συνέχιση των κύκλων.
Σε περίπτωση που η μοριακή ανάλυση διαπιστώνει μη μεθυλιωμένο υποκινητή του γονιδίου MGMT, τότε γνωρίζουμε ότι το καθιερωμένο σχήμα Stupp δεν είναι το ίδιο αποτελεσματικό, όπως σε ασθενείς με μεθυλιωμένο υποκινητή, και στην περίπτωση αυτή θα πρέπει να σκεφτούμε σοβαρά και διαφορετικές επιλογές χημειοθεραπείας.
Καινούργιες πειραματικές μέθοδοι, όπως η ανοσοθεραπεία εφαρμόζονται όλο και συχνότερα στην περίπτωση των γλοιοβλαστωμάτων.
Enciso-Mora V, Gousias K et al, Deciphering the 8q24.21 association for glioma. Hum mol Genet 2013;22(11):2293-2302.
Encisio-Mora V, Gousias K et al. Low penetrance susceptibility to glioma is caused by the TP53 variant rs78378222. Br J Cancer 2013;108(10):2178-2185.
Gousias K et al, Descriptive epidemiology of cerebral gliomas on northwest Greece and study of potential predisposing factors, 2005-2007. Neuroepidemiology 2009;33(2):89-95.
Gousias K et al, Nuclear karyopherin a2:a novel biomarker for infiltrative astrocytomas. Neurooncol 2012;109(3):545-553
Gousias K et al, Frequent abnormalities of the immune system in gliomas and correlation with the WHO grading system of malignancy. J Neuroimmunol 2010;226(1-2):136-142
Gousias K et al. Phenotypical analysis, relation to malignancy and prognostic relevance of ICOS+ T regulatory and dentritic cells in patients with gliomas. J Neuroimmunol 2013;264(1-2):84-90.
Gousias K et al. Extent of resection and survival in supratentorial infiltrative low-grade gliomas: analysis of and adjustment for treatment bias. Acta Neurochir.2014;156(2):327-337
Gousias K et al. Expertise in Surgical Neurooncology. Results of a survey of EANS Neurooncology Section. Brain and Spine 2024;4:102822
Gousias K et al. KPNA2 predicts long term survival in patients with anaplastic oligoastrocytomas. J Clin Neurosc 2014;21(10):1719-1724
Gousias K et al, Prognostic value of the preoperative immunological profile in patients with glioblastoma. Surg Neurol Int 2014; 5:89
Gousias K et al. Mechanisms of Cell Cycle Arrest and Apoptosis in Glioblastoma. Biomedicines 2022; 10(3):564
Gousias K et al. Resektionsausmaß und Prognose bei Gliomen; ‘‘Viel hilft viel‘‘ oder ‘‘alles oder nichts‘‘?, In. Simon M, Gliomchirurgie, Springer Verlag, 2018
Jacobs DI, Gousias K et al. Leveraging ethnic group incidence variation to investigate genetic susceptibility to glioma: a novel candidate SNP approach. Front Genet 2012; 3:2023
Kinnersley B, Gousias K et al, Quantifying the heritability of glioma using genome-wide complex trait analysis. Sci Rep 2015;4:17267
Kinnersley B, Gousias K et al, Genome-wide association study identifies multiple susceptibility loci for glioma. Nature Commun.2015;6:8559.
Kinnersley B, Gousias K et al.Search for new loci and low-frequency variants influencing glioma risk by exome-array analysis. Eur J Hum Genet 2016;24(5):717-724
Martinez R, Gousias K. Silencing of the nucleocytoplasmic shuttling protein karyopherin a2 promotes cell-cycle arrest and apoptosis in glioblastoma multiforme. Oncotarget 2018;9(71):33471-33481.
Louis DN et al, The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol 2021;23(8):1231-1251
Melin BS, Gousias K et al, Genome-wide association study of glioma subtypes identifies specific differences in genetic susceptibility to glioblastoma and non-glioblastoma tumors. Nature Genetics 2017;49(5):789-794.
Sanson M, Gousias K et al, Chromosome 7p11.2 (EGFR) variation influences glioma risk. Hum Mol Genet 2011;20(14):2897-2904
Simon M, Gousias K et al, Genetic risk profiles identify different molecular etiologies for glioma. Clin Cancer Res 2010;16(21):5252-5259
Simon M, Gousias K et al. TERT promoter mutations: a novel independent prognostic factor in primary glioblastomas.Neuro Oncol 2015;17(1):45-52
Stummer W et al, Extent of resection and survival in glioblastoma multiforme: identification of and adjustment for bias. Neurosurgery 2008;62(3):564-76
Wang XW, Gousias K et al, Prognostic impact of isocitrate dehydrogenase 1 singel-nucleotide polymorphism rs11554137 in malignant gliomas. Cancer 2013;119(4)806-813
Ostrom QT et al, CBTRUS Statistical Report: Primary Brain and Other Central Nervous System Tumors Diagnosed in the United States in 2016-2020. Neuro Oncol 2023;25(12 Suppl2):iv1-iv99.
Το γλοιοβλάστωμα είναι ο πιο συχνός και επιθετικός πρωτοπαθής κακοήθης όγκος του εγκεφάλου. Αναπτύσσεται από τα γλοιακά κύτταρα, τα οποία υποστηρίζουν και προστατεύουν τα νευρικά κύτταρα.
Το γλοιοσάρκωμα (gliosarcoma) είναι μια πιο επιθετική μορφή του γλοιοβλαστώματος, που χαρακτηρίζεται από μίξη διαφορετικών κυτταρικών τύπων. Συνήθως έχει παρόμοια ή και πιο δυσμενή πρόγνωση.
Το υποτροπιάζον γλοιοβλάστωμα είναι η επανεμφάνιση του όγκου μετά την αρχική θεραπεία (χειρουργείο, χημειοθεραπεία, ακτινοθεραπεία). Δυστυχώς, είναι συχνό φαινόμενο λόγω της επιθετικής φύσης του όγκου.
Δυστυχώς, ακόμη και μετά από πλήρη χειρουργική αφαίρεση, το γλοιοβλάστωμα έχει μεγάλη πιθανότητα υποτροπής. Για τον λόγο αυτό εφαρμόζεται συνδυαστικά και επικουρική θεραπεία, όπως ακτινοθεραπεία και χημειοθεραπεία.
Η χειρουργική αφαίρεση γλοιοβλαστώματος θεωρείται απαιτητική επέμβαση, καθώς ο όγκος μπορεί να βρίσκεται κοντά σε κρίσιμες περιοχές του εγκεφάλου (ομιλία, κίνηση, μνήμη). Η χρήση σύγχρονων τεχνικών, όπως νευροπλοήγηση, διεγχειρητική νευροπαρακολούθηση και χειρουργεία σε εγρήγορση, αυξάνει την ασφάλεια και τις πιθανότητες μέγιστης αφαίρεσης.
Το προσδόκιμο ζωής εξαρτάται από πολλούς παράγοντες: την ηλικία, τη γενική κατάσταση του ασθενούς, τα μοριακά χαρακτηριστικά του όγκου και κυρίως τον βαθμό αφαίρεσης. Mε πλήρη αφαίρεση, σωστή επικουρική θεραπεία και παρακολούθηση, ορισμένοι ασθενείς ζουν αρκετά χρόνια με καλή ποιότητα ζωής.